|
亙幚尡偱柧傜偐偵偟偨偄偙偲亜
僀僆儞壔孹岦傪乽戄偦偆偐傑偁偁偰偵偡偢側傂偳偡偓傞敀嬥乿偲妎偊偨恖偼懡偄偱偟傚偆丅偦傟偵傛傞偲 |
亙SACP (Sacrificial Anode Cathodic Protection) 偲偺娭學亜 嶬傃懳嶔偺媄弍偺拞偵 SACP 偲偄偆偺偑偁傝傑偡丅Faraday 偺巘偺 Davy 偑憂巒偟偨曽朄偱丄揝偺嶬傪杊偖偵偼揝傛傝僀僆儞壔孹岦偺戝偒偄嬥懏偲偮側偘偽傛偄偲偄偆傕偺偱偡丅 偦偺棫応偐傜偡傞偲乽巁偺拞偱垷墧偼揝傪庣偭偰偔傟傞偐?乿乽垷墧偼揝偺戙傢傝偵媇惖 sacrifice 偵側偭偰偔傟傞偐?乿偲偄偆栤偄偐偗偵側傝傑偡丅 |
|
亙幚尡偺庬椶亜
恾偺4庬椶偺幚尡傪傗傝傑偡丅M=Fe, N=Zn, A=5% 僋僄儞巁偱偡乮儗儌儞偺僋僄儞巁偼6乣7%偺傛偆偱偡乯丅
|
亙幚尡儌乕僪 1乣4亜
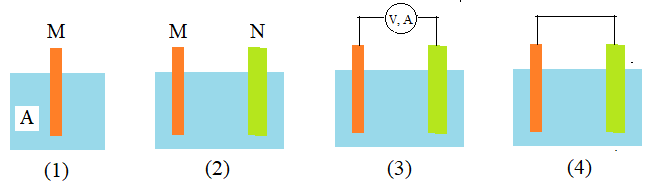
|
|
亙幚尡憰抲亜
|
亙幚尡憰抲偺恾亜

|