|
亙幚尡寢壥偺惍棟亜
幚尡儌乕僪偺恾傪嵞搙嶲徠偟側偑傜寢壥傪惍棟偟傑偡丅
|
亙幚尡儌乕僪亜
M=峾揝傑偨偼僗僥儞儗僗僗僠乕儖偺恓嬥 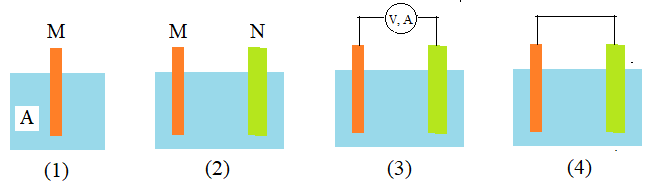
亙堄奜偩偭偨偙偲亜 婥懱偑敪惗偟偨偺偼丄N 傛傝僀僆儞壔孹岦偑彫偝偄 M 偐傜偩偭偨丅偨偩偟丄崁栚5偼僀僆儞壔孹岦偲柕弬偟側偄丅 |
|
亙斀墳儌僨儖亜
N 偲 M 偑夞楬偱偮側偑偭偰偄傞 Mode 3乣4 偵偮偄偰偼塃恾偺斀墳儌僨儖偑峫偊傜傟傑偡丅斀墳(1)偺揹巕偺嫙媼尦偼丄M偺尨巕偺僀僆儞壔偲Zn偺僀僆儞壔偺擇偮偁傝傑偡偑丄
屻幰偺傎偆偑偼傞偐偵惃偄偑偁傝傑偡丅 亙摍壙夞楬亜 r=亣偱旝彮揹棳丄r=0 偱嵟戝揹棳傪幚尰偡傞夞楬偲偟偰塃恾偑峫偊傜傟傑偡丅兿偺抣偼N偺桳柍偱曄偊傞昁梫偑偁傝傑偡丅 |
亙斀墳儌僨儖偲摍壙夞楬亜 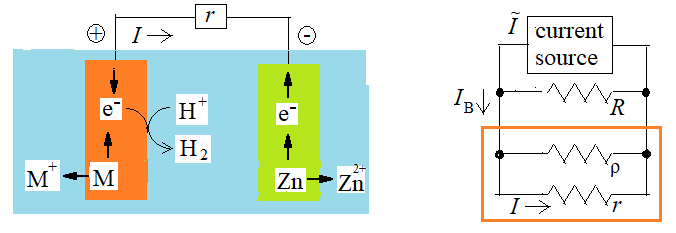
|
|
亙峾揝慄偺昞柺曄壔亜
堦楢偺幚尡傪廔偊偨屻偺峾揝慄偱偡丅枹巊梡偺慄偲斾妑偡傞偲崟壔偑栚棫偪傑偡丅 
|
亙傕偟奀悈拞傑偨偼怘墫悈拞偱幚尡偡傟偽亜 SACP 傪妋擣偡傞幚尡偵側傝傑偡丅Mode 1 偲 Mode 2 偱偼嶬傃偑敪惗偡傞偱偟傚偆丅傕偪傠傫婥朅偼敪惗偟傑偣傫丅 Mode 3 偲 Mode 4 偱偼嶬傃偑弌側偄偲婜懸偝傟傑偡丅抶偄曄壔側偺偱偡傋偰偺Mode傪摨偠忦審壓偱摨帪偵幚峴偡傋偒偱偟傚偆丅 |