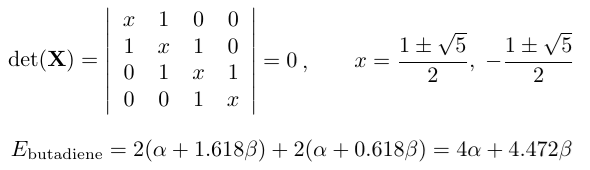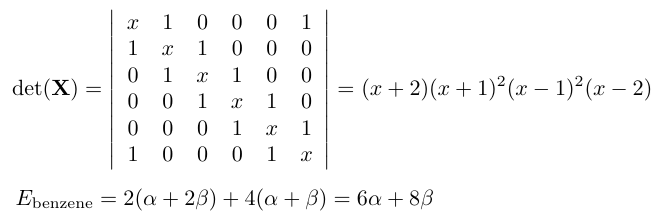|
<Hückel近似分子軌道法 (HMO)>
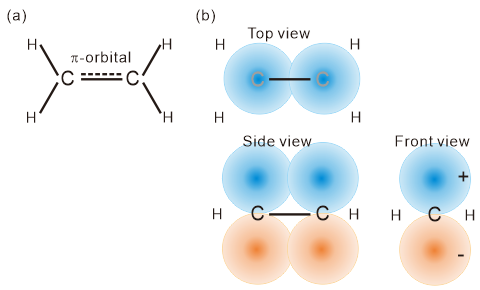
最も簡単なπ電子系はエチレンでしょう。右図(a)で直線はσ結合の化学結合、点線がπ結合を示します。両方合わせて二重結合ができます。図(b)はπ分子軌道(pi-MO)を様々な方向から眺めた図です。複素数なのであくまでも「感じ」です。このMOにはC-C軸上に節面がないので電子は二つのC原子の間を行き来して化学結合に寄与します(次のMOからは節面が現れます)。 もしMOが正確なら Hφj= Eφj というSchrödinger方程式を満足しますが実際には近似解 Ej=<φj|H|φj>/<φj|φj> しか得られません。そこでφjを原子軌道χiで展開してで最も良い近似値で満足することにします。こうしてx=(α-E)/β についての行列式が導かれます。ここでαはクーロン積分、βは共鳴積分(原子ij間に結合があれば取り入れる)と言います。 エチレンの場合、C1とC2にπ電子があるので右の行列式を解けば x=±1 です。x=-1にπ電子が2個入るので全エネルギーは右の通りです。 |
<エチレン CH2=CH2 のHMO>
|
|
<ブタジエン CH2=CH-CH=CH2 のHMO>
C1〜C4にπ電子があるので次の行列式と解が得られます。
エチレン2個分のエネルギーより 0.472β だけ低い(絶対値でいえば大きい) のはC2とC3の間にもπ結合ができているためです。このエネルギーを非局在化エネルギーといいます。 |
<ベンゼン C6H6 のHMO>
C1〜C6にπ電子があるので次の行列式と全エネルギーが得られます。 Kekulé構造(エチレン3個分)より 2β 低いことでいわゆる芳香族性が説明できます。 |
|
<Wolfram code (chemistry_hmo.nb)> (1) エチレンのπ電子エネルギー。次のコードで 2x2 の行列を定義し、表示し、行列式を解き、電子2個のエネルギーを算出します。

(2) ブタジエンのπ電子エネルギー。次のコードで 4x4 の行列を定義し、行列式を解きます。

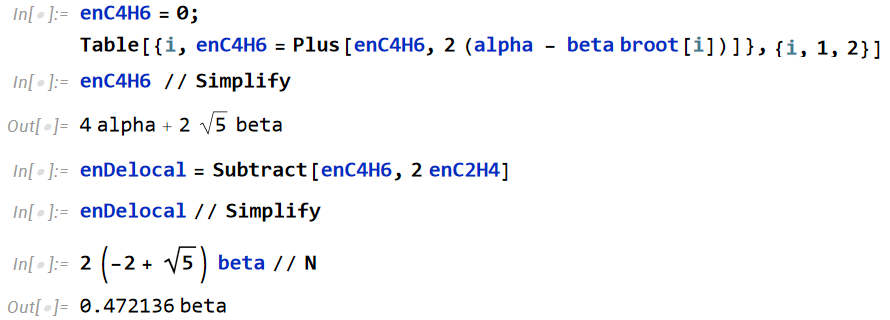
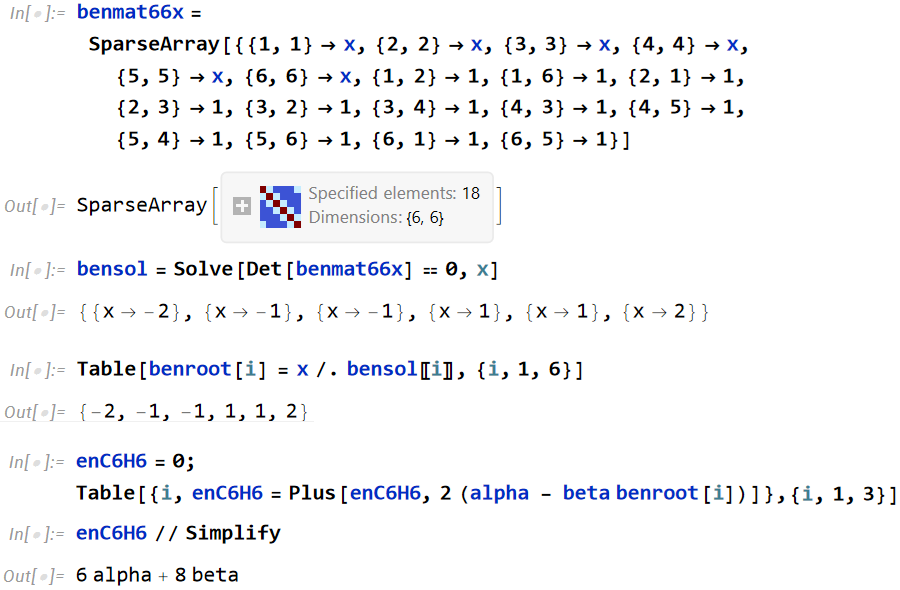
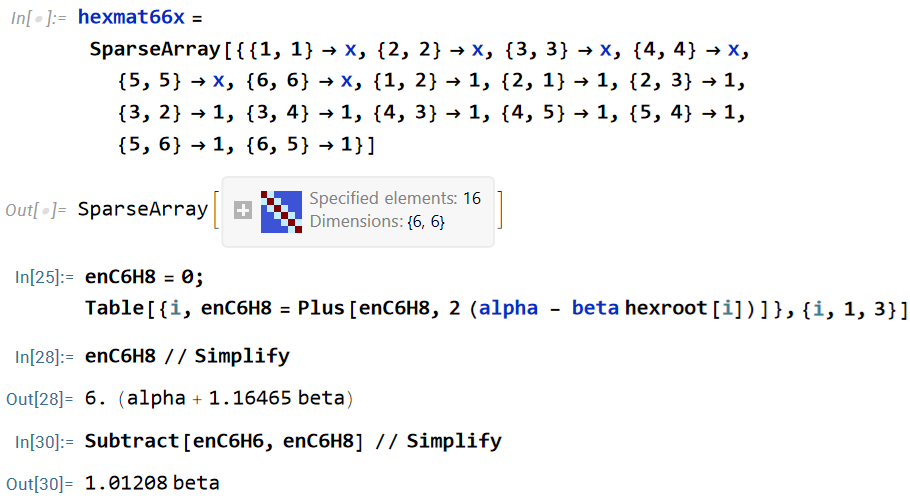
(3) ベンゼンのπ電子エネルギー。次のコードで 6x6 の行列を定義し、行列式を解き、π電子全部のエネルギーを出します。
| |